Укажите основные промышленные способы получения карбоновых кислот. Химические свойства карбоновых кислот
13.1.1. Окисление углеводородов . Существует два способа: окисление низших алканов C 4 -C 8 преимущественно до уксусной кислоты и окисление твердого парафина с образованием синтетических жирных кислот (СЖК) с прямой цепью углеродных атомов С 10 -С 20 , являющихся сырьем для синтеза ПАВ (поверхностно-активных веществ).
Процесс протекает в жидкой фазе при нагревании или в присутствии катализаторов. При окислении алканов происходит деструкция по связям между вторичными углеродными атомами, поэтому из н-бутана образуется главным образом уксусная кислота, а в качестве побочных продуктов – метилэтилкетон и этилацетат.
13.1.2.Синтезы на основе оксида углерода (II). Карбоновые кислоты получают на основе оксида углерода реакцией карбонилирования:
Присоединение по двойной связи при кислотном катализе всегда протекает по правилу Марковникова, вследствие этого только из этилена получается неразветвленная кислота, а из его гомологов - α-метилзамещенные кислоты. Особый интерес данный метод представляет для синтеза кислот с третичным радикалом (неокислот) из разветвленных олефинов (реакция Коха):

Механизм реакции состоит в предварительном протонировании алкена кислотой с образованием иона карбения, его взаимодействия с СО с получением ацилий – катиона и реакции последнего с водой с образованием карбоновой кислоты:
Неокислоты и их соли обладают очень высокой растворимостью и вязкостью, а их сложные эфиры - стабильностью к гидролизу, что обеспечивает им широкое применение в ряде отраслей.
Карбонилирование спиртов катализируется комплексами металлов (Ni, Со, Fe, Pd). Процесс реализован в промышленности для синтеза уксусной кислоты из метанола и характеризуется высокими экономическими показателями.
Кислоты также получают окислением альдегидов (продукт оксосинтеза).
Лабораторные способы получения карбоновых кислот
Окисление алканов.
Окисление алкенов.
13.2.3. Окисление первичных спиртов .
13.2.4. Окисление альдегидов и кетонов . Альдегиды окисляются значительно легче, чем кетоны. Кроме того, окисление альдегидов приводит к образованию кислот с тем же числом углеродных атомов, в то время как окисление кетонов протекает с разрывом углерод – углеродных связей (образуются две кислоты или кислота и кетон):

Окислителями служат перманганат или бихромат калия. Окисление кетонов требует более жестких условий, чем альдегидов.
13.2.5. Гидролиз нитрилов. Нитрилы получают взаимодействием галогеналканов с цианистым калием, проводят гидролиз водными растворами кислот или щелочей. В кислой среде азот выделяется в виде соли аммония:

в щелочной - в виде гидроксида аммония, который разлагается с выделением аммиака, кислота же получается в виде соли:

13.2.6. Синтез Гриньяра. При взаимодействии магнийорганических соединений с диоксидом углерода образуются соли карбоновых кислот:
Под действием сильной кислоты (обычно НСl) соль превращается в кислоту:
Гидролиз жиров
Жиры - сложные эфиры карбоновых кислот и глицерина (триглицериды). Карбоновые кислоты, входящие в состав жиров имеют углеродную цепь от 3 до 18 углеродных атомов.
Кипячение жиров или масел с водными растворами щелочей (NaOH, КОН) приводит к получению солей карбоновых кислот и глицерина.
Эта операция называется омылением, так как соли карбоновых кислот используют для изготовления мыла.
Гидролиз производных карбоновых кислот.
Физические свойства
Низшие кислоты с числом атомов углерода до 3 – легколетучие бесцветные жидкости с характерным острым запахом, смешиваются с водой в любых соотношениях. Большинство кислот С 4 – С 9 – маслянистые жидкости с неприятным запахом. Растворимость в воде сильно уменьшается с ростом молярной массы. Кислоты от С 10 и выше – твердые вещества, нерастворимые в воде. Плотности муравьиной и уксусной кислот больше единицы, остальных – меньше единицы. Температура кипения возрастает с увеличением молярной массы, при одном и том же числе углеродных атомов кислоты нормального строения кипят выше, чем кислоты с разветвленным углеродным скелетом. Сравнение температур кипения кислот и спиртов с одинаковым числом углеродных атомов показало, что кислоты кипят при значительно более высоких температурах, чем спирты. Это свидетельствует о более высокой ассоциации молекул кислот по сравнению со спиртами за счет образования водородных связей.
Карбоновые кислоты, как и спирты, способны образовывать водородные связи. Если акцептором является достаточно сильное основание, образование водородной связи предшествует полному переносу протона к основанию. По Бренстеду, соединение, являющееся донором водорода, считают «кислотой». Будет ли данное соединение «донором водорода» («кислотой»), зависит от природы «акцептора водорода» («основания»). Чем сильнее основание, тем больше вероятность того, что данное соединение будет вести себя по отношению к нему как кислота:

Межмолекулярные водородные связи, возникающие между молекулами карбоновых кислот, настолько прочны, что даже в газообразном состоянии значительная часть молекул существует в виде димеров:

С ростом углеводородной цепи способность кислот к образованию водородных связей уменьшается.
ОПРЕДЕЛЕНИЕ
Органические вещества, молекулы которых содержат одну или несколько карбоксильных групп, соединенных с углеводородным радикалом, называют карбоновыми кислотами .
Первые три члена гомологического ряда карбоновых кислот, включая пропионовую кислоту, — жидкости, имеющие резкий запах, хорошо растворимые в воде. Следующие гомологи, начиная с масляной кислоты, — также жидкости, обладающие резким неприятным запахом, но плохо растворимые в воде. Высшие кислоты, с числом атомов углерода 10 и более, представляют собой твердые вещества, без запаха, нерастворимые в воде. В целом, в ряду гомологов с увеличением молекулярной массы уменьшается растворимость в воде, уменьшается плотность и возрастает температура кипения (табл. 1).
Таблица 1. Гомологический ряд карбоновых кислот.
Получение карбоновых кислот
Карбоновые кислоты получают окислением предельных углеводородов, спиртов, альдегидов. Например, уксусную кислоту - окислением этанола раствором перманганата калия в кислой среде при нагревании:
Химические свойства карбоновых кислот
Химические свойства карбоновых кислот обусловлены в первую очередь особенностями их строения. Так, растворимые в воде кислоты способны диссоциировать на ионы:
R-COOH↔R-COO — + H + .
Благодаря наличию в воде иона H + они имеют кислый вкус, способны менять окраску индикаторов и проводить электрический ток. В водном растворе эти кислоты - слабые электролиты.
Карбоновые кислоты обладают химическими свойствами, характерными для растворов неорганических кислот, т.е. взаимодействуют с металлами (1), их оксидами (2), гидроксидами (3) и слабыми солями (4):
2CH 3 -COOh + Zn → (CH 3 COO) 2 Zn + H 2 (1);
2CH 3 -COOH + CuO→ (CH 3 COO) 2 Cu + H 2 O (2);
R-COOH + KOH → R-COOK + H 2 O (3);
2CH 3 -COOH + NaHCO 3 → CH 3 COONa + H 2 O + CO 2 (4).
Специфическое свойство предельных, а также непредельных карбоновых кислот, проявляемое за счет функциональной группы, — взаимодействие со спиртами.
Карбоновые кислоты взаимодействуют со спиртами при нагревании и в присутствии концентрированной серной кислоты. Например, если к уксусной кислоте прилить этиловый спирт и немного серной кислоты, то при нагревании появляется запах этилового эфира уксусной кислоты (этилацетата):
CH 3 -COOH + C 2 H 5 OH ↔CH 3 -C(O)-O-C 2 H 5 + H 2 O.
Специфическое свойство предельных карбоновых кислот, проявляемое за счет радикала, — реакция галогенирования (хлорирования).

Применение карбоновых кислот
Карбоновые кислоты служат исходным сырьем для получения кетонов, галогенангидридов, виниловых эфиров и других важных классов органических соединений.
Муравьиная кислота широко применяется для получения сложных эфиров, используемых в парфюмерии, в кожевенном деле (дубление кож), текстильной промышленности (как протрава при крашении), в качестве растворителя и консерванта.
Водный раствор (70-80%-ной) уксусной кислоты называется уксусной эссенцией, а 3-9%-ный водный раствор - столовым уксусом. Эссенция нередко используется для получения уксуса в домашних условиях путем разведения.
Примеры решения задач
ПРИМЕР 1
| Задание | С помощью каких химических реакций можно осуществить следующие превращения:
а) CH 4 → CH 3 Cl → CH 3 OH → HCHO → HCOOH → HCOOK. Напишите уравнения реакций, укажите условия их протекания. |
| Ответ | а) Хлорирование метана на свету приводит к получению хлорметана:
CH 4 + Cl 2 →CH 3 Cl + HCl. Галогенпроизводные алканов подвергаются гидролизу в водной или щелочной среде с образованием спиртов: CH 3 Cl + NaOH→CH 3 OH + NaCl. В результате окисления первичных спиртов, например, дихроматом калия в кислой среде в присутствии катализатора (Cu, CuO, Pt, Ag) образуются альдегиды: CH 3 OH+ [O] →HCHO. Альдегиды легко окисляются до соответствующих карбоновых кислот, например, перманганатом калия: HCHO + [O] →HCOOH. Карбоновые кислоты, проявляют все свойства, присущие слабым минеральным кислотам, т.е. способны взаимодействовать с активными металлами с образованием солей: 2HCOOH+ 2K→2HCOOK + H 2 . |
ПРИМЕР 2
| Задание | Напишите уравнения реакций между следующими веществами: а) 2-метилпропановой кислотой и хлором; б) уксусной кислотой и пропанолом-2; в) акриловой кислотой и бромной водой; г) 2-метилбутановой кислотой и хлоридом фосфора (V). Укажите условия протекания реакций. |
| Ответ | а) в результате реакции взаимодействия между 2-метилпропановой кислотой и хлором происходит замещение атома водорода в углеводородном радикале, находящемся в a-положение; образуется 2-метил-2-хлорпропановая кислота
H 3 C-C(CH 3)H-COOH + Cl 2 → H 3 C-C(CH 3)Cl-COOH + HCl (kat = P). б) в результате реакции взаимодействия между уксусной кислотой и пропанолом-2 происходит образование сложного эфира - изопропиловый эфир уксусной кислоты. CH 3 -COOH + CH 3 -C(OH)H-CH 3 → CH 3 -C(O)-O-C(CH 3)-CH 3 . в) в результате реакции взаимодействия между акриловой кислотой и бромной водой присоединение галогена по месту двойной связи в соответствии с правилом Марковникова; образуется 2,3-дибромпропановая кислота CH 2 =CH-COOH + Br 2 → CH 2 Br-CHBr-COOH г) в результате реакции взаимодействия между 2-метилбутановой кислотой и хлоридом фосфора (V) образуется соответствующий хлорангидрид CH 3 -CH 2 -C(CH 3)H-COOH + PCl 5 →CH 3 -CH 2 -C(CH 3)H-COOCl + POCl 3 + HCl. |
Получение карбоновых кислот
I . В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
2. Окисление алканов:
2CH 4 + + 3O 2 t,kat → 2HCOOH + 2H 2 O
метан муравьиная кислота
2CH 3 -CH 2 -CH 2 -CH 3 + 5O 2 t,kat,p → 4CH 3 COOH + 2H 2 O
н-бутан уксусная кислота
3. Окисление алкенов:
CH 2 =CH 2 + O 2 t,kat → CH 3 COOH
этилен
СH 3 -CH=CH 2 + 4[O] t,kat → CH 3 COOH + HCOOH (уксусная кислота+муравьиная кислота )
4. Окисление гомологов бензола (получение бензойной кислоты):
C 6 H 5 -C n H 2n+1 + 3n[O] KMnO4,H+ → C 6 H 5 -COOH + (n-1)CO 2 + nH 2 O
5C 6 H 5 -CH 3 + 6KMnO 4 + 9H 2 SO 4 → 5C 6 H 5 -COOH + 3K 2 SO 4 + 6MnSO 4 + 14H 2 O
толуол бензойная кислота
5. Получение муравьиной кислоты:
1 стадия: CO + NaOH t , p → HCOONa ( формиат натрия – соль )
2 стадия : HCOONa + H 2 SO 4 → HCOOH + NaHSO 4
6. Получение уксусной кислоты:
CH 3 OH + CO t,p → CH 3 COOH
Метанол
II . В лаборатории
1. Гидролиз сложных эфиров:
2. Из солей карбоновых кислот :
R-COONa + HCl → R-COOH + NaCl
3. Растворением ангидридов карбоновых кислот в воде:
(R-CO) 2 O + H 2 O → 2 R-COOH
4. Щелочной гидролиз галоген производных карбоновых кислот:

III . Общие способы получения карбоновых кислот
1. Окисление альдегидов:
R-COH + [O] → R-COOH
Например, реакция «Серебряного зеркала» или окисление гидроксидом меди (II ) – качественные реакции альдегидов
2. Окисление спиртов:
R-CH 2 -OH + 2[O] t,kat → R-COOH + H 2 O
3. Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода.

4. Из цианидов (нитрилов) – способ позволяет наращивать углеродную цепь:
СH 3 -Br + Na-C≡N → CH 3 -CN + NaBr
CH 3 —CN — метилцианид (нитрил уксусной кислоты)
СH 3 -CN + 2H 2 O t → CH 3 COONH 4
ацетат аммония
CH 3 COONH 4 + HCl → CH 3 COOH + NH 4 Cl
5. Использование реактива Гриньяра
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Число карбоксильных групп характеризует основность кислоты.
В зависимости от количества карбоксильных групп карбоновые кислоты подразделяются на одноосновные карбоновые кислоты (содержат одну карбоксильную группу), двухосновные (содержат две карбоксильные группы) и многоосновные кислоты.
В зависимости от вида радикала, связанного с карбоксильной группой, карбоновые кислоты делятся на предельные, непредельные и ароматические. Предельные и непредельные кислоты объединяют под общим названием кислоты алифатического или жирного ряда.
Одноосновные карбоновые кислоты
1.1 Гомологический ряд и номенклатура
Гомологический ряд одноосновных предельных карбоновых кислот (иногда их называют жирными кислотами) начинается с муравьиной кислоты
Формула гомологического ряда
Номенклатура ИЮПАК разрешает сохранять для многих кислот их тривиальные названия, которые обычно указывают на природный источник, из которого была выделена та или иная кислота, например, муравьиная, уксусная, масляная, валериановая и т.д.
Для более сложных случаев названия кислот производят от названия углеводородов с тем же числом атомов углерода, что и в молекуле кислоты, с добавлением окончания -овая и слова кислота. Муравьиная кислота Н-СООН называется метановой кислотой, уксусная кислота СН 3 -СООН - этановой кислотой и т. д.
Таким образом, кислоты рассматриваются как производные углеводородов, одно звено которых превращено в карбоксил:

При составлении названий кислот с разветвленной цепью по рациональной номенклатуре их рассматривают как производные уксусной кислоты, в молекуле которой атомы водорода замещены радикалами, например, триметилуксусная кислота (СН 3) 3 С – СООН.
1.2 Физические свойства карбоновых кислот
Только с чисто формальных позиций можно рассматривать карбоксильную группу как комбинацию карбонильной и гидроксильной функций. Фактически их взаимное влияние друг на друга таково, что полностью изменяет их свойства.
Обычная для карбонила поляризация двойной связи С=0 сильно возрастает за счет дополнительного стягивания свободной электронной пары с соседнего атома кислорода гидроксильной группы:

Следствием этого является значительное ослабление связи О-Н в гидроксиле и легкость отщепления атома водорода от него в виде протона (Н +). Появление пониженной электронной плотности (δ+) на центральном углеродном атоме карбоксила приводит также к стягиванию σ-электронов соседней связи С-С к карбоксильной группе и появлению (как у альдегидов и кетонов) пониженной электронной плотности (δ +) на α-углеродном атоме кислоты.
Все карбоновые кислоты обладают кислой реакцией (обнаруживается индикаторами) и образуют соли с гидроксидами, оксидами и карбонатами металлов и с активными металлами:
Карбоновые кислоты в большинстве случаев в водном растворе диссоциированы лишь в малой степени и являются слабыми кислотами, значительно уступая таким кислотам, как соляная, азотная и серная. Так, при растворении одного моля в 16 л воды степень диссоциации муравьиной кислоты равна 0,06, уксусной кислоты - 0,0167, в то время как соляная кислота при таком разбавлении диссоциирована почти полностью.
Для большинства одноосновных карбоновых кислот рК а = 4,8, только муравьиная кислота имеет меньшую величину рК а (около 3,7), что объясняется отсутствием электронодонорного эффекта алкильных групп.
В безводных минеральных кислотах карбоновые кислоты протонируются по кислороду с образованием карбкатионов:

Сдвиг электронной плотности в молекуле недиссоциированной карбоновой кислоты, о котором говорилось выше, понижает электронную плотность на гидроксильном атоме кислорода и повышает ее на карбонильном. Этот сдвиг еще больше увеличивается в анионе кислоты:
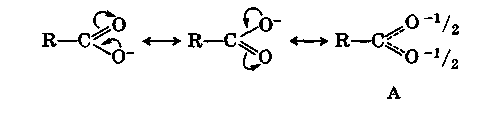
Результатом сдвига является полное выравнивание зарядов в анионе, который фактически существует в форме А - резонанс карбоксилат-аниона.
Первые четыре представителя ряда карбоновых кислот - подвижные жидкости, смешивающиеся с водой во всех отношениях. Кислоты, в молекуле которых содержится от пяти до девяти атомов углерода (а также изомасляная кислота), - маслянистые жидкости, растворимость их в воде невелика.
Высшие кислоты (от С 10) - твердые тела, практически нерастворимы в воде, при перегонке в обычных условиях они разлагаются.
Муравьиная, уксусная и пропионовая кислоты имеют острый запах; средние члены ряда обладают неприятным запахом, высшие кислоты запаха не имеют.

На физических свойствах карбоновых кислот сказывается значительная степень ассоциации вследствие образования водородных связей. Кислоты образуют прочные водородные связи, так как связи О-Н в них сильно поляризованы. Кроме того, карбоновые кислоты способны образовывать водородные связи с участием атома кислорода карбонильного диполя, обладающего значительной электроотрицательностью. Действительно, в твердом и жидком состоянии карбоновые кислоты существуют в основном в виде циклических димеров:
Такие димерные структуры сохраняются в некоторой степени даже в газообразном состоянии и в разбавленных растворах в неполярных растворителях.
